

抗アレルギー作用と治療薬
抗アレルギー作用とアレルギー反応のメカニズム
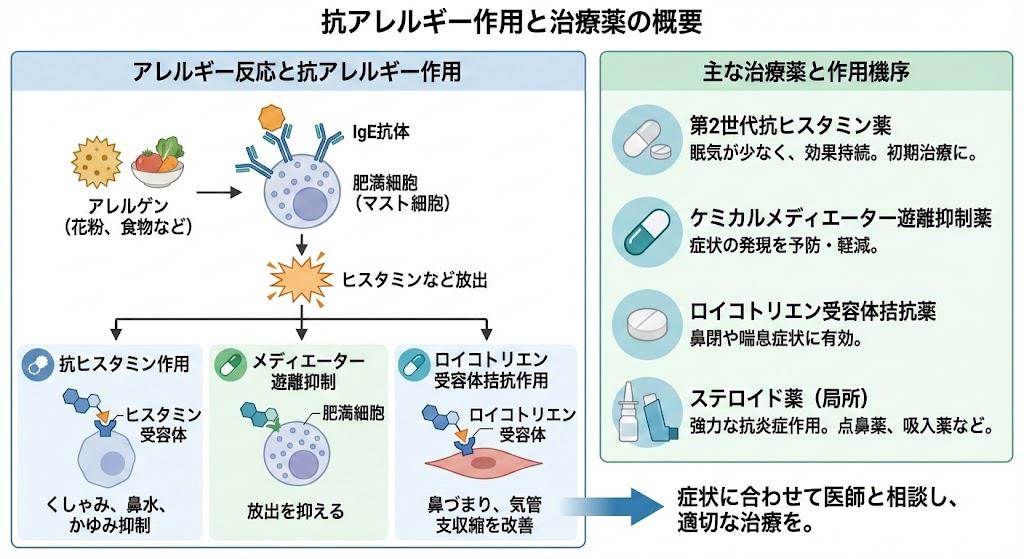
アレルギー反応は、本来無害なはずの物質(アレルゲン)に対して免疫系が過剰に反応することで起こります。この反応の中心となるのが「肥満細胞」と呼ばれる免疫細胞です。アレルゲンが体内に侵入すると、肥満細胞の表面にあるIgE抗体と結合し、複数のIgE抗体受容体が連結(架橋)することで肥満細胞が活性化されます。
活性化された肥満細胞は「脱顆粒」と呼ばれる現象を起こし、ヒスタミンをはじめとする様々な化学伝達物質(メディエーター)を放出します。これらの物質が血管透過性の亢進や平滑筋の収縮などを引き起こし、アレルギー症状として現れるのです。
抗アレルギー作用とは、このアレルギー反応のいずれかの段階を抑制する働きを指します。具体的には以下の2つの主要なアプローチがあります。
- ヒスタミン受容体の遮断:すでに放出されたヒスタミンの作用を抑える
- 肥満細胞からの化学伝達物質遊離抑制:そもそもヒスタミンなどの放出を防ぐ
これらの作用機序を理解することが、効果的なアレルギー治療の基盤となります。
抗アレルギー作用を持つヒスタミン受容体拮抗薬の種類
ヒスタミン受容体は体内に複数のタイプが存在し、それぞれ異なる生理作用を担っています。現在までに同定されているのは主にH1、H2、H3、H4の4種類です。アレルギー症状に最も関連が深いのはH1受容体で、これを遮断する薬剤が抗ヒスタミン薬として広く使用されています。
第一世代抗ヒスタミン薬
古典的な抗ヒスタミン薬として知られるこれらの薬剤は、H1受容体に高い親和性を持ちますが、血液脳関門を通過しやすいため中枢神経系にも作用し、眠気などの副作用が強く出る傾向があります。
代表的な薬剤。
- レスタミン(ジフェンヒドラミン)
- タベジール(クレマスチン)
- ポララミン(d-クロルフェニラミン)
- ペリアクチン(シプロヘプタジン)
第二世代抗ヒスタミン薬
血液脳関門を通過しにくく設計されており、中枢神経系への作用が少ないため眠気などの副作用が軽減されています。また、一部の薬剤は肥満細胞からのメディエーター遊離抑制作用も併せ持ちます。
代表的な薬剤。
- アレグラ(フェキソフェナジン):眠気が最も少ないが効果も比較的穏やか
- クラリチン(ロラタジン):1日1回の服用で済む
- ジルテック(セチリジン):効果が強いが個人差で眠気が出ることも
- アレロック(オロパタジン):効果が強く、アトピー性皮膚炎にも使用される
- ザイザル(レボセチリジン):セチリジンの改良型で効果が強い
- アレジオン(エピナスチン):効果発現が早く眠気も少ない
抗アレルギー作用における肥満細胞の役割と制御機構
肥満細胞はアレルギー反応の中心的な役割を担う免疫細胞です。皮膚や粘膜組織に広く分布し、アレルゲンに対する最初の防御線として機能します。しかし、アレルギー疾患ではこの肥満細胞の過剰な活性化が問題となります。
肥満細胞の活性化メカニズム
肥満細胞の表面にはIgE抗体を捕捉するための高親和性受容体(FcεRI)が発現しています。アレルゲンがこの受容体に結合したIgE抗体と架橋結合すると、細胞内でシグナル伝達が起こり、細胞質内の顆粒に蓄えられていたヒスタミンやトリプターゼなどの化学伝達物質が放出されます。
肥満細胞の制御を目指した抗アレルギー薬
肥満細胞からの化学伝達物質の遊離を抑制する作用を持つ薬剤は、アレルギー反応の初期段階で介入するため、より根本的な治療アプローチとなります。これらの薬剤は「メディエーター遊離抑制薬」とも呼ばれ、以下のような作用機序があります。
- 細胞内カルシウムイオンの流入阻害
- cAMPの上昇による脱顆粒抑制
- 細胞内シグナル伝達経路の阻害
代表的な薬剤としては、クロモグリク酸ナトリウム(インタール)やトラニラスト(リザベン)などがあります。これらは即効性はありませんが、継続的に使用することでアレルギー症状の予防に効果を発揮します。
最近の研究では、短鎖脂肪酸が肥満細胞の活性化を抑制する効果があることが明らかになっています。東京理科大学の西山千春教授らの研究グループによると、短鎖脂肪酸は肥満細胞の細胞膜上のGPR109Aに結合し、プロスタグランジンE2の産生を促進することで肥満細胞の脱顆粒を抑制するという新たなメカニズムが解明されました。
抗アレルギー作用とH1・H2受容体の併用療法の効果
アレルギー治療において、H1受容体拮抗薬(抗ヒスタミン薬)が第一選択薬として広く使用されていますが、特に難治性の蕁麻疹などでは単剤での効果が不十分な場合があります。そこで注目されているのが、H1受容体拮抗薬とH2受容体拮抗薬(H2ブロッカー)の併用療法です。
H1・H2受容体の分布と機能
ヒスタミン受容体の分布は体内の組織によって異なります。
- H1受容体:血管内皮細胞、中枢神経、気管支などに広く分布
- H2受容体:胃壁細胞、平滑筋、リンパ球、そして重要なことに皮膚の血管内皮細胞にも存在
この分布の違いが、併用療法の理論的根拠となっています。
併用療法の作用機序
H1・H2受容体拮抗薬の併用が効果的である理由は主に3つあります。
- 受容体の包括的遮断:皮膚の血管内皮細胞にはH1とH2の両方の受容体が存在するため、両方を遮断することでヒスタミンの作用をより効果的に抑制できます。
- 薬物代謝の相互作用:H2ブロッカーは肝臓での薬物代謝を阻害する作用があり、これによりH1受容体拮抗薬の血中濃度が上昇し、効果が増強されます。
- 免疫調節作用:H2ブロッカーには細胞免疫を高める作用があり、IgEなどの抗体産生(体液性免疫)を抑制することでアレルギー症状を軽減します。
臨床エビデンス
2012年にFedorowiczらが行ったコクランレビューでは、慢性蕁麻疹に対するH1・H2受容体拮抗薬の併用療法の有効性が報告されています。特に通常の抗ヒスタミン薬で効果が不十分な難治性の蕁麻疹に対して、この併用療法が有効であることが示されています。
実際の臨床では、アレグラ(フェキソフェナジン)などのH1受容体拮抗薬と、ガスター(ファモチジン)などのH2ブロッカーを組み合わせて処方されることがあります。
抗アレルギー作用とヒスタミンH4受容体の新たな治療標的
近年の研究により、従来知られていたH1、H2、H3受容体に加えて、新たにH4受容体が同定され、アレルギー疾患の病態における重要な役割が明らかになってきました。H4受容体は主に免疫系細胞に発現しており、アレルギー反応の新たな治療標的として注目を集めています。
H4受容体の特徴と分布
H4受容体は以下のような特徴を持っています。
- 主に肥満細胞、好酸球、樹状細胞、T細胞などの免疫細胞に発現
- ヒスタミンに対する親和性がH1、H2受容体よりも高い
- Gαi/oタンパク質と共役し、細胞内カルシウム動員を引き起こす
H4受容体とアレルギー疾患
H4受容体は免疫細胞の遊走や活性化に関与しており、アレルギー性炎症の増幅に重要な役割を果たしています。特に以下のような作用が報告されています。
- 好酸球や肥満細胞の組織への遊走促進
- T細胞の活性化と炎症性サイトカイン産生
- 樹状細胞の活性化とアレルゲン提示能の増強
- 痒みの感覚伝達への関与
H4受容体拮抗薬の開発状況
H4受容体の発見を受けて、選択的H4受容体拮抗薬の開発が進められています。前臨床試験では、これらの化合物が以下のような効果を示すことが報告されています。
- アレルギー性気道炎症の軽減
- 皮膚炎症と痒みの抑制
- 好酸球性炎症の抑制
- 自己免疫疾患モデルでの効果
特に注目すべきは、H4受容体拮抗薬が従来の抗ヒスタミン薬では効果が限定的だったアトピー性皮膚炎の痒みに対して有効である可能性が示されていることです。アトピー性皮膚炎では、肥満細胞由来のトリプターゼによるPAR2受容体を介する痒みや、Th2細胞が産生するIL-31による痒みなど、ヒスタミン以外の経路も重要であることが知られていますが、H4受容体はこれらの経路とも相互作用している可能性があります。
現在、いくつかのH4受容体拮抗薬が臨床試験段階にあり、今後のアレルギー治療の新たな選択肢として期待されています。